AUFGABENSTELLUNG
Biofunktionalisierte Implantatmaterialien sind mit einer biologisch wirksamen Komponente ausgerüstet, die von körpereigenen Zellen aktiv erkannt wird. Dadurch werden im Wundgewebe Zellreaktionen wie Adhäsion oder Proliferation verstärkt und auf diese Weise der Einheilungs- und Regenerationsprozess beschleunigt. Genau wie nicht-funktionalisierte Implantate sind diese Materialien Medizinprodukte und unterliegen damit den entsprechenden gesetzlichen Anforderungen. Unter anderem bedeutet das, dass vor dem Einsatz eine Sterilisation zwingend notwendig ist. Die gängigsten Sterilisationsverfahren für Medizinprodukte sind bislang die Dampfsterilisation, die Strahlensterilisation (β und g) sowie die Sterilisation mit Ethylenoxid. Bei metallischen oder permanenten polymeren Materialien sind diese Methoden erprobt und effektiv. Bei Implantaten aus leicht degradierbaren oder thermolabilen Polymeren und Biopolymeren besteht jedoch die Gefahr der Schädigung, da hohe Temperaturen (Dampf), energiereiche Strahlung (g-Sterilisation) oder aggressive Reagenzien (Ethylenoxid) auf die Struktur und Integrität der Materialien destruktiv wirken können. Zudem sind die in den biofunktionalisierten Produkten eingesetzten biologisch aktiven Komponenten zur Erzeugung des gewünschten Effekts auf eine intakte dreidimensionale Konformation angewiesen. Eine Schädigung des Materials durch harsche Sterilisationsbedingungen kann daher vielfältige negative Folgen haben. Dazu zählen das Versagen des Implantats oder eine längere Einheilungsphase, was wiederum die Lebensqualität der Patienten beeinträchtigt sowie erhöhte Therapiekosten nach sich zieht. Sollen solche Implantate vor dem Einsatz sterilisiert werden, muss dies mit einer Methode geschehen, die die strukturelle Integrität gewährleistet und insbesondere die Funktionalität der bioaktiven Substanzen nicht beeinträchtigt.
PROJEKTZIEL | ARBEITSHYPOTHESE
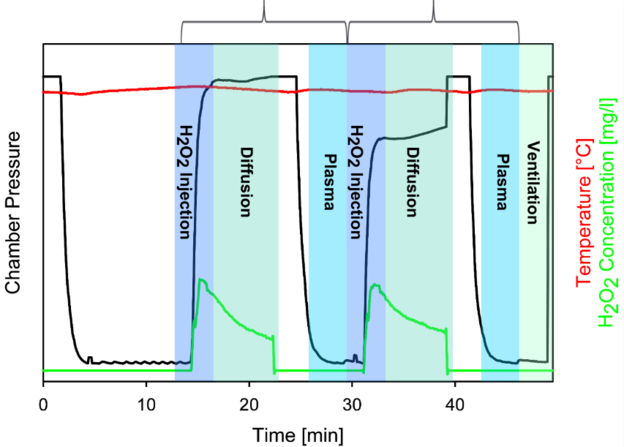
Ziel des Projekts ist die Entwicklung eines Sterilisationsprozesses, der auf thermisch labile Implantatmaterialien mit bioaktiven Oberflächen angewendet werden kann und dabei die mechanischen und biologischen Funktionalitäten dieser Materialien weitestgehend erhält. Basierend auf dem Wasserstoffperoxid-Gas-Plasmaverfahren soll der Prozess für biofunktionalisierte Medizinprodukte optimiert und beispielhaft an mit Wachstumsfaktoren beschichteten PLA- und PCL-Folien etabliert werden.
NUTZEN | AUSBLICK
Bei erfolgreicher Realisierung bietet das zu entwickelnde Sterilisationsverfahren erhebliche Vorteile gegenüber den bisher üblicherweise angewendeten Methoden. Herstellern von biofunktionalisierten Implantaten oder anderen biologischen Medizinprodukten stünde ein materialschonender Sterilisationsprozess zur Verfügung, der kostengünstig, mit wenig technischem Aufwand, dezentral vor Ort, zeitnah und prozessbegleitend durchgeführt werden kann. Die bei g-Bestrahlung oder Behandlung mit Ethylenoxid üblichen Laufzeiten von 1 bis 3 Wochen würden entfallen. Zudem wird bislang bei der Funktionalisierung von Implantaten mit Wachstumsfaktoren ein Überschuss der biologisch aktiven Komponente eingesetzt, um so deren Verlust durch die Sterilisation auszugleichen. Bei Anwendung des zu entwickelnden Verfahrens kann die eingesetzte Menge an teuren Wachstumsfaktoren kostensparend reduziert werden. Und auch für FuE-Einrichtungen bietet ein dezentraler und materialschonender Sterilisationsprozess die Möglichkeit, Forschungsaktivitäten zu erleichtern und zu beschleunigen.
FORMALE ANGABEN | PROJEKTLEITER FILK | PROJEKTPARTNER |
Programm: INNO-KOM Förderkennzeichen: 49MF210048 Projektbeginn: 11.2021 Laufzeit: 30 Monate | Carolin Großmann Franziska Ullm Dr. Enno Klüver | keine |